•Notícia
Cèl·lules programables
Detectar agents tòxics, generar energies netes o produir medicaments a gran escala són algunes de les nombroses possibilitats de la biologia sintètica, una jove disciplina científica busca com transformar les cèl·lules en petits ordinadors biològics programats per desenvolupar tasques predeterminades.
La biologia sintètica tot just va començar a desenvolupar-se ara fa uns vuit anys. De fet, és una branca de la ciència tan nova que encara no té una definició consolidada. Una primera manera d’entendre-la és adoptar un punt de vista molt microscòpic i fonamental, fins a cert punt molt químic, és a dir, sintetitzar noves molècules (per exemple, nucleòtids) amb significat biològic. En l’altre extrem se situa la visió de la biologia sintètica, que se centra en el nivell dels organismes, cosa que significa crear formes de vida noves (per exemple, virus).
A mig camí entre aquests dos camps de recerca hi ha una altra subdisciplina “més prometedora, des del punt de vista que ens pot ajudar a entendre els sistemes vius, centrada en la creació de nous circuits genètics —formats per gens i proteïnes que interaccionen de manera complexa— que es poden introduir en les cèl·lules, amb la finalitat que funcionin de manera diferent a com ho farien en el seu context original, així com en l’estandardització d’aquests circuits per poder-los combinar després entre si”, explica Jordi García Ojalvo, investigador del Departament de Física i Enginyeria Nuclear al Campus de Terrassa de la UPC.
Un dels objectius actuals de la biologia és arribar a conèixer com funcionen els circuits genètics que regulen l’activitat de les cèl·lules. Per respondre a aquesta qüestió es pot adoptar l’estratègia que triaria un enginyer: “Si vols entendre com funciona una cosa, construeix-la, és a dir, si vols entendre com una cèl·lula fa una cosa, construeix un circuit que faci aquesta cosa”, puntualitza García Ojalvo. A parer seu, el que es coneix amb el nom de ciències dures, que fins ara es dedicaven a estudiar la matèria inerta, pot fer un paper important en l’estudi de la matèria viva.
La implicació d’una persona en aquesta formació, que sap com funcionen aquests mecanismes en altres tipus de sistemes, és molt adequada, per exemple, per agafar un circuit, crear un model matemàtic mitjançant una simulació per ordinador i analitzar-lo. D’aquesta manera és possible deduir quines són les condicions que necessita un circuit per poder fer una cosa determinada.
D’altra banda, avui dia hi ha moltes tècniques i dispositius que encara necessiten persones expertes en física i enginyeria per poder-les desenvolupar, com ara aconseguir tenir les cèl·lules en un entorn ben controlat (microfluídica) o veure-les amb més precisió (òptica). Tot això, sense oblidar els coneixements i les dades que, evidentment, proporciona un biòleg. És en aquest sentit que es diu que la biologia sintètica és intrínsecament interdisciplinària.
Però aquesta àrea de coneixement no parteix de zero. Ha recollit els fruits dels treballs realitzats al llarg de les últimes dècades en camps com ara l’enginyeria genètica, la biologia molecular i, més recentment, la biologia de sistemes. Concretament, quant als avenços que n’han permès el desenvolupament, cal destacar el descobriment de la proteïna verda fluorescent i la seva utilització com a marcador que permet estudiar nombrosos processos en totes les àrees de la biologia, una tècnica que ha esdevingut rutinària i que permet visualitzar què fa cada cèl·lula en resposta a alguna cosa, quin és el seu estat en temps real.
Una de les grans novetats que aporta aquesta disciplina és la interiorització d’un concepte: l’estandardització. Si es fes un símil amb l’electrònica, es podria dir que de la mateixa manera que un disc dur serveix per a qualsevol ordinador, els circuits genètics es podrien introduir en qualsevol cèl·lula per desenvolupar una tasca concreta.
Per fer tot això, en comptes de provar d’entendre els circuits genètics complexos que existeixen a la naturalesa, la biologia sintètica proposa una altra manera d’afrontar el repte: construir circuits genètics tan senzills com sigui possible, entendre com funcionen i incrementar-ne el nivell de complexitat pas a pas. En tractar-se de circuits senzills, en què només estan implicats dos o tres gens, és possible desenvolupar models matemàtics que no tan sols permeten predir el comportament de la cèl·lula pel que fa al grau de producció de proteïnes, sinó també induir en la cèl·lula una dinàmica determinada.
Això és precisament el que va fer l’any 2000 el grup de recerca de Michael Elowitz, del California Institute of Technology, que va construir el primer oscil·lador o rellotge genètic sintètic. Amb aquesta fita, que va suposar l’inici d’aquesta nova àrea de coneixement científic, es va demostrar que les cèl·lules tenen un rellotge intern, és a dir, que calculen el temps i que es podrien sincronitzar per desenvolupar accions predeterminades.
Des d’aleshores, la recerca a Espanya es du a terme de la mà de grups científics com ara el de Dinàmica no Lineal, Òptica no Lineal i Làsers, del Campus de Terrassa, coordinat per Ramon Vilaseca i en el qual treballa García Ojalvo, entre altres investigadors. El grup fa recerca en biologia sintètica i biologia de sistemes des de fa sis anys, primer teòricament i des de fa dos anys també en l’àmbit experimental. L’equip desenvolupa la seva tasca en col·laboració amb el grup d’Elowitz i amb el de Gurol Suel, del Southwestern Medical Center de Dallas, per entendre processos de diferenciació —com canvien d’estat— en els bacteris, els organismes model que permeten estudiar funcions que es donen en organismes més complexos.
El mateix equip també col·labora amb el grup d’Alfonso Martínez Arias, de la University of Cambridge, per entendre el procés mitjançant el qual les cèl·lules mare embrionàries mantenen la pluripotencialitat, quin és el mecanisme que fa que conservin la capacitat de diferenciació en qualsevol tipus de cèl·lula. En aquest camp concret, no utilitzen la biologia sintètica per se, no construeixen circuits, sinó que intenten analitzar com funcionen els que ja existeixen a la naturalesa. Malgrat que, ara per ara, el treball del grup de la UPC no està determinat per cap aplicació concreta, l’objectiu final és arribar a controlar el comportament cel·lular externament, a voluntat.
Un dels aspectes més destacables de la biologia sintètica, tal com la conceben molts investigadors, és el fet que ens pot ajudar a entendre els organismes vius. Des d’aquest punt de vista, pot arribar a ser una eina fonamental per comprendre el funcionament de la maquinària cel·lular, ja que permet veure què es pot fer amb els components responsables de les funcions biològiques. De fet, permet acostar-se a la biologia des d’un punt de vista més quantitatiu per fer prediccions amb models que després s’han de comprovar al laboratori.
El repte que es planteja és enorme, sobretot si es té en compte que, per exemple, el genoma humà conté uns 30.000 gens, i una cèl·lula, al voltant d’un milió de proteïnes. Però una cèl·lula és quelcom més que la suma de les seves parts, i el seu funcionament s’ha d’entendre des del punt de vista del conjunt dels components. Aquests gens i aquestes proteïnes estan connectats entre si a través de milions de connexions.
Ara per ara, la finalitat no és cap altra que satisfer la curiositat, augmentar progressivament el coneixement científic sobre què poden fer quan interaccionen i definir i caracteritzar aquest flux d’informació que determina la posada en marxa d’un procés biològic com si es tractés d’un plànol.
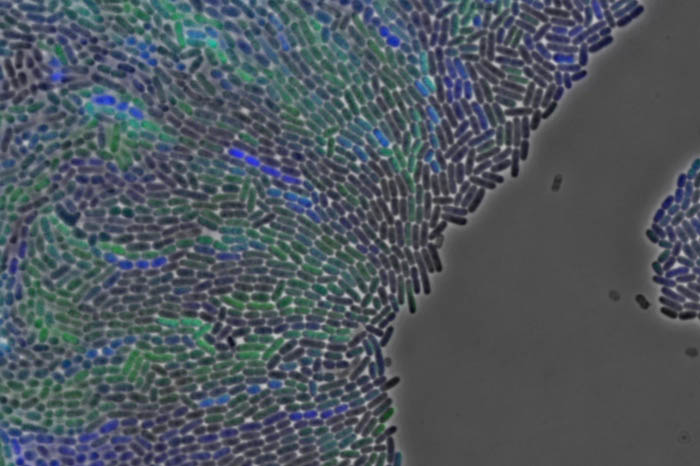
Detall de cèl·lules d'E.coli, que contenen dues proteïnes fluorescents són iscogèniques però actuen de manera diferent, la qual cosa dóna pistes als científics per saber com funcionen.
Quan es parla de les expectatives que genera el desenvolupament de la biologia sintètica —i sens dubte una de les àrees d’interès principal és la biomedicina—, els experts remarquen que no es tracta d’aplicacions a curt termini. No obstant això, ja n’hi ha exemples rellevants en el camp de la síntesi de nous medicaments: un equip del Lawrence Berkeley National Laboratory de Califòrnia ha reconstruït en el bacteri E. coli el circuit genètic encarregat de la síntesi del precursor de l’artemisina, un fàrmac contra la malària, amb l’objectiu de produir-lo de manera més eficient i a baix cost.
És potser en l’àmbit del medi ambient, que les aplicacions tenen unes perspectives de desenvolupament més imminents. S’està treballant, per exemple, en el disseny de microorganismes més eficients en la descontaminació d’ecosistemes (bioremediació).
En aquest mateix camp també es desenvolupen biosensors, que són dispositius capaços de reconèixer substàncies o microorganismes d’interès i d’interaccionar- hi.
Segueix-nos a Twitter


















